發布時間:2022-07-29
邁威生物 (688062.SH),一家全產業鏈布局的創新型生物制藥公司,宣布其自主研發的靶向 Nectin-4 ADC 創新藥(研發代號:9MW2821)臨床試驗申請正式獲得美國食品藥品監督管理局 (FDA) 的批準,可針對實體瘤患者開展臨床試驗。9MW2821 是國內同靶點藥物中首個開展臨床試驗的品種,已在國內多地醫院開展 I 期臨床試驗。
9MW2821 是邁威生物利用國際領先的抗體偶聯藥物 (Antibody Drug Conjugate, ADC) 開發平臺和自動化高通量雜交瘤抗體分子發現平臺開發的一款靶向 Nectin-4 ADC 創新藥,用于治療實體瘤。該品種通過具有自主知識產權的偶聯技術連接子及優化的 ADC 偶聯工藝,實現抗體的定點修飾。9MW2821 可與腫瘤細胞表面的 Nectin-4 結合并進入腫瘤細胞,定向釋放細胞毒素,從而實現對腫瘤的精準殺傷。
此外,9MW2821 具有組分均一,純度較高以及便于產業化等特點。非臨床研究表明,其在多個腫瘤模型中均具有良好的腫瘤抑制效果,并且在食蟹猴、小鼠的體內安全性研究中表現出更好的治療窗口,目前該項目已有多項臨床研究在國內同步開展。
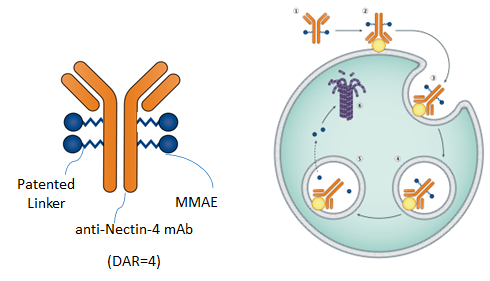
圖片來源:The biology and rationale of targetingnectin-4 in urothelial carcinoma. Nature reviews Urology 2021
邁威生物聯合創始人、CEO 劉大濤博士表示:“9MW2821 的研發進展在全球同靶點 ADC 藥物中位居前列,這體現了我們在創新藥研發方面的實力。邁威生物憑借行業經驗豐富的資深團隊與深厚的研發實力,建立了包括 ADC 開發平臺在內的多個國際領先的研發平臺,9MW2821 是國內首個靶向 Nectin-4 ADC 創新藥品種,在實體瘤的治療方面擁有廣闊的應用前景。ADC 藥物因其精準殺傷癌細胞的特點,近年來逐漸成為國內創新藥的熱門領域。邁威生物始終致力于開發具備臨床差異化價值的生物創新藥,解決全球患者未被滿足的臨床需求。”